Dott.ssa Antonella Coretti Medico Chirurgo – Specialista in Pediatria / Pneumologia Pediatrica. Impegnata nella ricerca e nella gestione clinica delle patologie respiratorie croniche infantili. Membro attivo della SIMRI (Società Italiana per le Malattie Respiratorie Infantili), collabora alla definizione di percorsi diagnostici per la cronicità aerodigestiva:
- Expertise: Atresia Esofagea, Tracheomalacia, Follow-up respiratorio nel prematuro.
- Affiliazioni: Ospedale Pediatrico Bambin Gesù
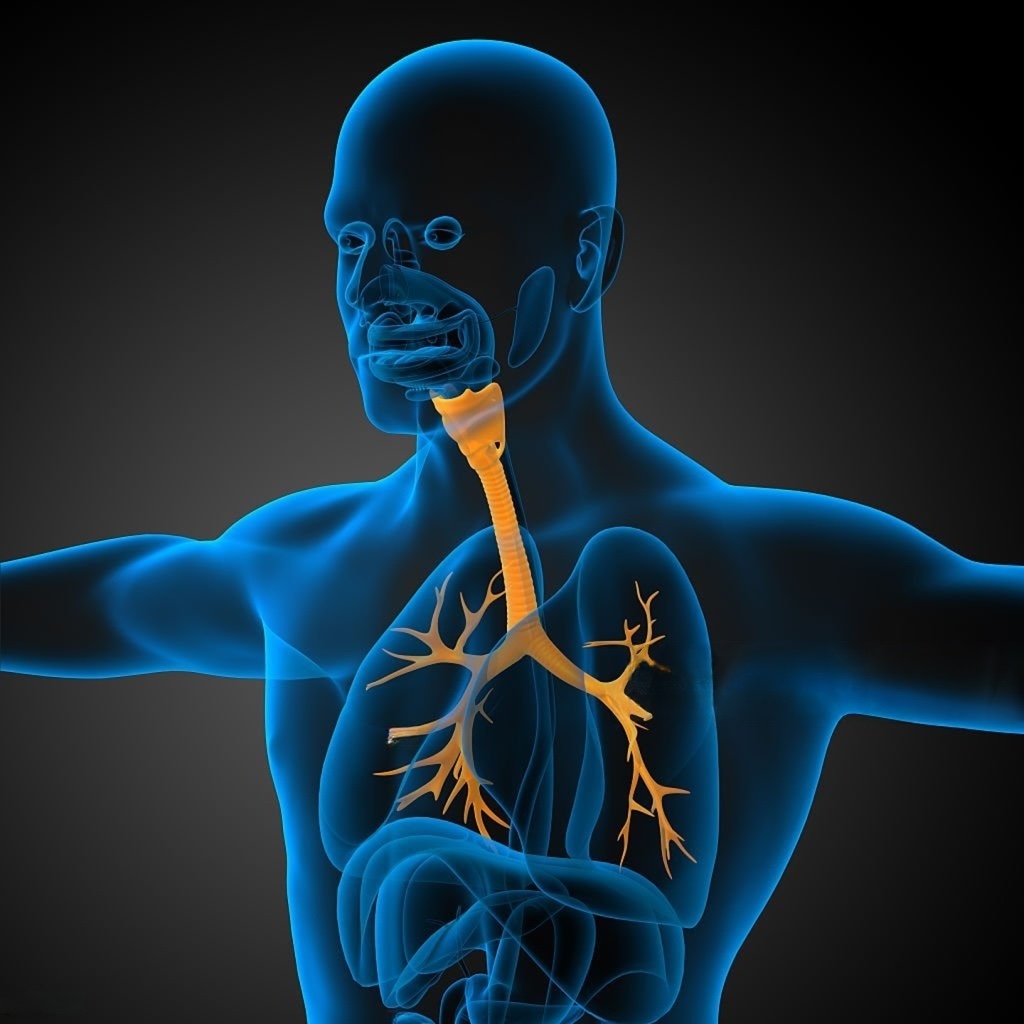
L’atresia esofagea (AE), spesso associata a fistola tracheoesofagea (TEF), rappresenta una malformazione congenita complessa che coinvolge lo sviluppo embrionale dell’apparato digerente e respiratorio. Grazie ai progressi della chirurgia neonatale e delle cure intensive, la sopravvivenza dei pazienti con atresia esofagea con o senza fistola tracheoesofagea (AE/TEF), ha raggiunto tassi prossimi al 100%. Tuttavia, numerosi studi dimostrano che l’AE non può considerarsi risolta con l’intervento chirurgico, ma essa rappresenta una condizione cronica, caratterizzata da una complessa morbilità aerodigestiva a lungo termine che comprende disfagia, malattia da reflusso gastroesofageo (GERD), stenosi anastomotiche ricorrenti, tracheomalacia e infezioni polmonari recidivanti. La gestione di questa “cronicità aerodigestiva” impone un modello di follow-up a lungo termine e multidisciplinare che preveda l’integrazione di chirurghi, gastroenterologi, pneumologi e logopedisti, con l’obiettivo di prevenire danni parenchimali polmonari irreversibili e migliorare la qualità della vita del paziente.
Complicanze post-operatorie: Stenosi anastomotica, malattia da reflusso gastroesofageo e disfagia
La gestione multidisciplinare dell’atresia esofagea è essenziale per prevenire l’impatto del bolo alimentare e garantire una corretta crescita ponderale nei primi anni di vita. Dopo la riparazione chirurgica dell’AE/TEF una delle complicanze più frequenti è la stenosi anastomotica a livello dell’esofago, che deriva dalla cicatrizzazione del sito di unione dei segmenti esofagei. Queste stenosi possono richiedere dilatazioni ripetute, spesso con tecniche di endoscopic balloon dilatation, che risultano efficaci e sicure anche nei neonati di basso peso – Cho J. Y. et al., 2022. Oltre alla stenosi, tra le complicanze più comuni si rileva la malattia da reflusso gastroesofageo (GERD) e la disfagia – Friedmacher et al., 2017.
Complicanze digestive a lungo termine: stenosi anastomotica, disfagia cronica e malattia da reflusso gastroesofageo
L’intervento chirurgico risolve l’interruzione meccanica dell’esofago, ma non può correggere le anomalie funzionali intrinseche dell’organo malformato. In questo contesto, la dismotilità esofagea è un elemento costante e pervasivo, derivante da un alterato controllo neurologico e da una distribuzione anomala delle fibre muscolari, condizioni già presenti alla nascita.
Stenosi anastomotica e disfagia cronica
La stenosi nel sito dell’anastomosi si verifica in circa il 26-50% dei pazienti operati per AE – Comella et al., 2021. Essa deriva da un processo di cicatrizzazione esuberante alimentato dalla tensione tissutale durante la riparazione chirurgica e dal reflusso acido. I pazienti manifestano disfagia, vomito ed episodi di impatto del bolo alimentare che possono richiedere procedure in urgenza per la rimozione endoscopica. Tutto ciò influenza negativamente la crescita nei primi anni di vita – Arroyo et al., 2023. Il trattamento d’elezione è la dilatazione endoscopica, che spesso richiede più sedute prima della risoluzione completa. Sebbene la stenosi anastomotica rappresenti una causa importante di disfagia, questa non è esclusivamente correlata alla presenza di una stenosi meccanica. Un ruolo centrale è svolto dalla dismotilità esofagea congenita – Christophe et al., 2017. L’alterata o assente peristalsi esofagea compromette il transito del bolo alimentare e la clearance esofagea, determinando disfagia anche in assenza di restringimenti anatomici significativi. A ciò si aggiungono il GERD, l’esofagite cronica, eventuali alterazioni sensoriali esofagee e, in alcuni casi, fattori neuromuscolari o respiratori associati.
Malattia da reflusso gastroesofageo
Il GERD colpisce oltre il 50% dei pazienti operati di AE/TEF- Aksionchyk et al., 2020. L’eziologia è multifattoriale:
- dismotilità esofagea congenita: è indipendente dalla tecnica chirurgica. La peristalsi inefficace o assente è causa di clearance esofagea ridotta, con conseguente stasi del contenuto, che favorisce il reflusso prolungato e il danno mucoso – Faure et al., 2017.
- alterazioni anatomiche post-chirurgiche: l’esofago ricostruito è spesso più corto e la tensione sull’anastomosi altera l’angolo di His e la funzione antireflusso. L’ipotonia dello sfintere esofageo inferiore contribuisce alla risalita del contenuto gastrico, soprattutto post-prandiale. L’esofago operato presenta una alterata sensibilità, può essere ipersensibile o, al contrario, poco sensibile – Van Wijk et al., 2013.
- svuotamento gastrico ritardato: favorisce la distensione gastrica e può predisporre a reflusso acido – Van Wijk et al., 2013.
Il reflusso persistente non è solo un problema di comfort, ma un catalizzatore di morbilità aerodigestiva che conduce a:
- Esofagite e stenosi peptiche: l’acido danneggia la mucosa, favorendo fibrosi e restringimenti.
- Esofago di Barrett: la sostituzione dell’epitelio squamoso normale dell’esofago da parte di epitelio colonnare (gastrico o intestinale), è stata riportata anche in età pediatrica e adolescenziale, e rappresenta un fattore di rischio significativo per l’adenocarcinoma esofageo in età adulta – Tullie et al., 2021.
- Microaspirazioni: il contenuto gastrico refluisce e, a causa della clearance inefficace, viene aspirato nelle vie aeree, alimentando la cascata respiratoria.
Le linee guida ESPGHAN-NASPGHAN raccomandano una terapia soppressiva acida aggressiva con inibitori di pompa protonica (PPI) per tutti i neonati operati, da proseguire per almeno il primo anno di vita, e un monitoraggio a lungo termine tramite pH-impedenzometria ed endoscopie seriali. Il trattamento chirurgico mediante fundoplicatio viene preso in considerazione nei pazienti con AE e GERD refrattario alla terapia medica ottimale o con complicazioni gravi documentate (esofagite severa persistente, complicanze respiratorie correlate, dipendenza cronica da terapia).
GERD e disfagia, quindi, oltre a presentarsi come conseguenze a breve termine, persistono dopo anni dalla riparazione dell’AE in una alta percentuale di pazienti. La dismotilità esofagea congenita, in quanto caratteristica intrinseca dell’AE, è l’elemento chiave nella genesi dei sintomi a lungo termine – Friedmacher et al., 2017. Tale disfunzione motoria compromette il transito del bolo alimentare e favorisce il reflusso, aumentando il rischio di aspirazione.
Fattori di rischio per la morbilità digestiva
Lo studio di Lu et al. (2021) identifica i principali fattori di rischio per lo sviluppo di morbilità digestiva dopo la riparazione dell’AE. Tra i fattori associati a un aumento del rischio di GERD, stenosi esofagea e necessità di interventi ripetuti, emergono la presenza di fistola tracheoesofagea distale, una lunga distanza tra i monconi esofagei (long-gap esophageal atresia) e la comparsa di complicanze postoperatorie precoci. Inoltre il GERD rappresenta un nodo centrale nella cascata di complicanze aerodigestive, fungendo da fattore predisponente sia per sintomi digestivi che per manifestazioni respiratorie legate all’aspirazione. Il reflusso persistente può infatti aggravare la dismotilità esofagea, favorire l’esofagite e aumentare il rischio di aspirazione cronica, con conseguenze respiratorie a lungo termine – Ebbott et al., 2025; Kovesi et al., 2004.
Complicanze respiratorie a lungo termine: il peso della tracheomalacia e dell’infiammazione cronica
Le problematiche respiratorie rappresentano una importante causa di morbilità e ospedalizzazione nei pazienti sottoposti a correzione di AE/TEF. Queste derivano da una complessa interazione tra anomalie strutturali congenite (sviluppo embrionale comune di esofago e trachea predispongono ad anomalie delle vie aeree, come tracheomalacia), esiti chirurgici (diverticoli tracheali, stenosi o fistole ricorrenti aggravano il rischio di ostruzione delle vie aeree e infezioni) e disturbi funzionali (disfunzione motoria esofagea e GERD concorrono all’aspirazione di contenuto gastrico, con conseguente infiammazione polmonare e infezioni ricorrenti) – Ebbott et al., 2025.
Le infezioni respiratorie ricorrenti, la tosse cronica, l’asma, la bronchite persistente e l’apnea ostruttiva del sonno, sono tra le complicanze respiratorie a lungo termine più frequenti nei pazienti con AE/TEF – Kovesi et al., 2004. I sintomi respiratori coesistono frequentemente con quelli digestivi e tendono a persistere nel tempo.
Tracheomalacia e instabilità dinamica
La tracheomalacia (TM) è presente nella quasi totalità dei pazienti con AE. Si tratta di una debolezza intrinseca della parete tracheale caratterizzata da sviluppo incompleto o anomalo della cartilagine e da una membrana posteriore (pars membranacea) notevolmente lassa. La TM, determina una ridotta stabilità delle vie aeree che porta a un collasso dinamico della trachea soprattutto durante l’espirazione, il pianto, la tosse o gli sforzi respiratori. Come descritto dalla European Respiratory Society, sulla base di quanto rilevato all’esame endoscopico, la TM può essere classificata in:
- lieve: riduzione del lume compresa tra 50% e 74%
- moderata: riduzione del lume compresa tra 75% e 89%
- severa: riduzione del lume compresa tra 90% e 100%
Dal punto di vista clinico, la TM si manifesta con la tipica “tosse abbaiante” (barky cough) e stridore. Nei casi severi, il collasso tracheale impedisce l’efficace clearance delle secrezioni, predisponendo a bronchiti batteriche ricorrenti, polmoniti e apnee ostruttive.
Asma, iperreattività bronchiale e aspirazione
In presenza di GERD e disfagia, le microaspirazioni croniche di contenuto gastrico contribuiscono all’infiammazione delle vie aeree, creando un circolo vizioso tra apparato digerente e respiratorio – Kovesi et al., 2017. Molti pazienti con AE ricevono una diagnosi di asma a causa di respiro sibilante e tosse cronica. Tuttavia, alcuni studi evidenziano che non è chiaro se l’uso di broncodilatatori sia associato a reale beneficio clinico in questi pazienti poiché molti sintomi derivano da cause anatomiche (es. tracheomalacia) e non da broncospasmo tipico dell’asma – Kovesi et al, 2013; Cartabuke et al. 2015; Ebbott et al, 2025. L’uso di broncodilatatori in questi pazienti richiede estrema cautela: sebbene possano alleviare la componente di broncostruzione, il rilassamento della muscolatura liscia bronchiale e tracheale potrebbe esacerbare il collasso dinamico dovuto alla malacia, peggiorando paradossalmente il quadro ostruttivo – Koumbourlis, et al., 2020. La gestione pneumologica deve quindi focalizzarsi sulla prevenzione dell’aspirazione, sull’igiene bronchiale e sull’uso mirato di corticosteroidi inalatori se è dimostrata una componente di iperreattività bronchiale o asma confermata da test funzionali (spirometria con reversibilità) – Koumbourlis, et al., 2020
Esiti funzionali e qualità della vita percepita dal paziente
Oltre agli esiti clinici oggettivi, la letteratura sottolinea l’importanza di considerare la percezione soggettiva del paziente. L’indagine condotta da Acher et al (2016) tramite comunità online di pazienti con AE/TEF, mostra che una percentuale significativa di soggetti riferisce sintomi aerodigestivi persistenti in età adulta, con un impatto rilevante sulla vita quotidiana. Le difficoltà di alimentazione, il reflusso e i problemi respiratori cronici, influenzano le relazioni sociali e il benessere psicologico, anche in assenza di complicanze considerate severe dal punto di vista clinico, evidenziando una possibile discrepanza tra le valutazioni cliniche e la percezione soggettiva del paziente.
La discordanza tra gli esiti clinici oggettivi e la qualità della vita percepita è un tema centrale della ricerca moderna. Le associazioni di pazienti, come F.AT.E. (Associazione Famiglie con Atresia Esofagea), che spesso raccolgono testimonianze e dati sulle esperienze vissute, riflettono come questa condizione impatta sulla qualità di vita dei pazienti e delle loro famiglie.
Alimentazione e impatto psicosociale
Le difficoltà alimentari influenzano non solo lo stato nutrizionale, ma anche le relazioni sociali. Il timore di episodi di soffocamento o la necessità di tempi lunghi per consumare un pasto, possono portare ad ansia sociale e isolamento. Nei bambini, questo può tradursi in un rifiuto del cibo o in comportamenti selettivi che complicano la gestione familiare.
Protocolli di follow-up multidisciplinare e standard di cura
La complessità delle complicanze aerodigestive richiede l’abbandono di una gestione frammentata a favore di un approccio integrato e a lungo termine – Ebbott et al., 2025.
La complessità della patologia aerodigestiva
La Consensus Conference di ERNICA (European Reference Network for Rare Inherited Congenital Anomalies) sottolinea la necessità di centralizzare le cure in centri ad alto volume e di istituire programmi di transizione verso la medicina dell’adulto.
La sorveglianza integrata gastroenterologica e pneumologica
Per affrontare in modo coordinato le difficoltà respiratorie e di deglutizione sono necessarie valutazioni aerodigestive che prevedano l’integrazione di gastroenterologi, pneumologi, foniatri e chirurghi pediatrici.
Il monitoraggio deve comprendere:
- Valutazione della deglutizione: studi videofluoroscopici per identificare rischi di aspirazione silente
- Monitoraggio della funzionalità respiratoria: spirometrie, studi del sonno e monitoraggio delle infezioni respiratorie ricorrenti. Nei casi sospetti di TM severa, la broncoscopia rimane il gold standard diagnostico.
- Sorveglianza endoscopica: biopsie esofagee periodiche per monitorare l’infiammazione e la trasformazione metaplasica, indipendentemente dalla presenza di sintomi, data la frequente discordanza tra clinica ed istologia nei pazienti con AE.
La figura del coordinatore aerodigestivo diventa fondamentale per sincronizzare gli interventi dei vari specialisti garantendo che ogni aspetto della patologia sia affrontato tempestivamente.
Sintesi delle evidenze e conclusioni cliniche
L’atresia esofagea è un paradigma della complessità in pediatria, dove il successo tecnico della chirurgia neonatale deve essere sostenuto da una visione prognostica a lungo termine. Le complicanze aerodigestive non sono eventi isolati, ma manifestazioni di un’alterazione sistemica che coinvolge l’apparato respiratorio e digerente e che tende a persistere e, in alcuni casi, ad evolvere negativamente con l’età.
La letteratura scientifica più recente e le consensus internazionali concordano sui seguenti pilastri gestionali:
- Centralizzazione delle cure: i pazienti devono essere seguiti in centri di riferimento che garantiscano l’integrazione tra specialità chirurgiche e mediche.
- Proattività diagnostica: non attendere la comparsa di sintomi severi per eseguire screening endoscopici o prove di funzionalità respiratoria, data la scarsa correlazione tra percezione del paziente e danno tissutale.
- Follow-up multidisciplinare e a lungo termine: sono necessarie valutazioni specialistiche che coinvolgano chirurghi pediatrici, gastroenterologi, pneumologi e specialisti della deglutizione. Il monitoraggio regolare della funzione esofagea e respiratoria consente di identificare precocemente le complicanze e di ridurre il rischio di danni cronici.
- Supporto Psicosociale: riconoscere l’impatto della patologia sulla vita quotidiana e fornire supporto psicologico costante sia al bambino che alla famiglia per affrontare le sfide della cronicità.
In definitiva, l’obiettivo ultimo della medicina moderna nell’AE/TEF non è più solo “far sopravvivere” il neonato, ma garantire una transizione verso l’età adulta priva di disabilità respiratorie e con una qualità della vita sovrapponibile a quella della popolazione generale. La pubblicazione di protocolli chiari e aggiornati su portali come SIMRI.it è un passo fondamentale per standardizzare le cure e promuovere la ricerca clinica di eccellenza in questo campo.
Bibliografia
Cho JY, Chang MY, Gang MH et al. Postoperative Complications of Esophageal Atresia and Role of Endoscopic Balloon Dilatation in Anastomotic Strictures. Pediatr Gastroenterol Hepatol Nutr. 2022 Nov;25(6):453-460. doi: 10.5223/pghn.2022.25.6.453.
Ebbott D, Maddahi Y, Fall F, et al. Long-term aerodigestive morbidities after esophageal atresia/tracheoesophageal fistula repair. J Pediatr Surg. 2025;60(8):162384. doi:10.1016/j.jpedsurg.2025.162384.
Acher CW, Ostlie DJ, Leys CM, et al. Long-Term Outcomes of Patients with Tracheoesophageal Fistula/Esophageal Atresia: Survey Results from Tracheoesophageal Fistula/Esophageal Atresia Online Communities. Eur J Pediatr Surg. 2016 Dec;26(6):476-480. doi: 10.1055/s-0035-1570103. Epub 2015 Dec 21.PMID: 26692337.
Lu YH, Yen TA, Chen CY, et al. Risk factors for digestive morbidities after esophageal atresia repair. Eur J Pediatr. 2021 Jan;180(1):187-194. doi: 10.1007/s00431-020-03733-1. Epub 2020 Jul 9.PMID: 32648144.
Friedmacher F, Kroneis B, Huber-Zeyringer A, et al. Postoperative Complications and Functional Outcome after Esophageal Atresia Repair: Results from Longitudinal Single-Center Follow-Up. J Gastrointest Surg. 2017 Jun;21(6):927-935. doi: 10.1007/s11605-017-3423-0. Epub 2017 Apr 19.PMID: 28424985.
Kovesi T, Rubin S. Long-term complications of congenital esophageal atresia and/or tracheoesophageal fistula. Chest. 2004 Sep;126(3):915-25. doi: 10.1378/chest.126.3.915.PMID: 15364774 Review.
Krishnan U, Mousa H, Dall’Oglio L, et al. ESPGHAN-NASPGHAN Guidelines for the Evaluation and Treatment of Gastrointestinal and Nutritional Complications in Children With Esophageal Atresia-Tracheoesophageal Fistula. JPGN Volume 63, Number 5, November 2016.
Van Wijk M, Knüppe F, Omari T, et al. Evaluation of gastroesophageal function and mechanisms underlying gastroesophageal reflux in infants and adults born with esophageal atresia. J Pediatr Surg. 2013 Dec;48(12):2496-505. doi: 10.1016/j.jpedsurg.2013.07.024.
Faure C, Righini Grunder F. Dysmotility in Esophageal Atresia: Pathophysiology, Characterization, and Treatment. Front. Pediatr. 5:130. doi: 10.3389/fped.2017.00130
Aksionchyk M, Marakhouski K, Svirsky A. Gastroesophageal reflux disease in pediatric esophageal atresia: Assessment of clinical symptoms and pH-impedance data. World J Clin Pediatr 2020 September 19; 9(2): 29-43. doi: 10.5409/wjcp.v9.i2.29
Comella A, Tanny S P T, Hutson J M, et al. Esophageal morbidity in patients following repair of esophageal atresia: A systematic review. J Pediatr Surg. 2021 Sep;56(9):1555-1563. doi: 10.1016/j.jpedsurg.2020.09.010.
Christophe F, Grunder F R et al. Dysmotility in Esophageal Atresia: Pathophysiology, Characterization, and Treatment. Front Pediatr. 2017 May 31;5:130. doi: 10.3389/fped.2017.00130
Kovesi T. Aspiration Risk and Respiratory Complications in Patients with Esophageal Atresia. Front Pediatr. 2017 Apr 3;5:62. doi: 10.3389/fped.2017.00062
Kovesi T. Long-term respiratory complications of congenital esophageal atresia with or without tracheoesophageal fistula: an update. Dis Esophagus. 2013 May-Jun;26(4):413-6. doi: 10.1111/dote.12061. 26(4), 413–416.
Koumbourlis A, Belessis Y, Cataletto M, et al. Care Recommendations for the Respiratory Complications of Esophageal Atresia-Tracheoesophageal Fistula: The International Network of Esophageal Atresia, Respiratory Complications Working Group. Authorea. June 05, 2020. DOI: 10.22541/au.159136783.30583958
Cartabuke R H, Lopez R, Thota P N. Long-term esophageal and respiratory outcomes in children with esophageal atresia and tracheoesophageal fistula. Gastroenterol Rep (Oxf). 2015 Oct 16;4(4):310–314. doi: 10.1093/gastro/gov055
Tullie L, Kelay A, Bethell G S et al. Barrett’s oesophagus and oesophageal cancer following oesophageal atresia repair: a systematic review. BJS Open. 2021 Jul 6;5(4):zrab069. doi: 10.1093/bjsopen/zrab069.
Moduli di risposte a richieste primarie
1. Inquadramento clinico e codici ufficiali
L’atresia esofagea è classificata come malattia rara (Codice esenzione: RN0160). La diagnosi postnatale si conferma con l’impossibilità di far passare un sondino radio-opaco oltre i 10 cm dalla bocca, validata da radiografia toraco-addominale.
| Parametro | Identificativo Ufficiale | Note |
| Codice Esenzione | RN0160 | Valido per Atresia Esofagea e/o Fistola TE |
| ICD-10 | Q39.0 (senza fistola), Q39.1 (con fistola) | Classificazione internazionale |
| ORPHA Code | 1199 | Portale Orphanet per le malattie rare |
| Associazione VACTERL | RN1250 | Co-occorrenza in circa il 25% dei casi |
2. Complicanze digestive e dismotilità esofagea
Modulo Answer-First: Circa il 50% dei pazienti operati sviluppa malattia da reflusso gastroesofageo (GERD) severa. La causa primaria è la dismotilità esofagea congenita, caratterizzata da peristalsi inefficace o assente, che compromette la clearance acida e favorisce stenosi anastomotiche.
Analisi delle complicanze gastrointestinali
| Complicanza | Incidenza Stimata | Fattori di Rischio |
| GERD | >50% | Dismotilità congenita, alterazione angolo di His |
| Stenosi Anastomotica | 26−50% | Tensione tissutale, reflusso acido persistente |
| Disfagia Cronica | Frequente | Stenosi meccanica o dismotilità pura |
| Esofago di Barrett | Variabile | Reflusso cronico non trattato (rischio oncologico) |
3. Morbilità respiratoria e Tracheomalacia
Modulo Answer-First: La tracheomalacia (TM) è presente nella quasi totalità dei pazienti AE/TEF. Si manifesta con la tipica “tosse abbaiante” (barky cough) e può causare collassi dinamici della trachea durante l’espirazione o lo sforzo, portando ad apnee ostruttive e infezioni respiratorie ricorrenti.
Classificazione ERS/ERNICA della Tracheomalacia
| Grado di TM | Riduzione del Lume Tracheale | Sintomatologia Tipica |
| Lieve | 50−74% | Stridore occasionale, tosse metallica |
| Moderata | 75−89% | Difficoltà respiratoria sotto sforzo |
| Severa | 90−100% | Apnee, cianosi, bradicardia, distress severo |
Nota Pneumologica: L’uso di broncodilatatori deve essere valutato con estrema cautela: rilassando la muscolatura liscia, possono esacerbare il collasso della parete tracheale malacica.
4. Reti Europee e PDTA Regionali
Modulo Answer-First: Il follow-up dei pazienti AE deve avvenire in centri ad alto volume inseriti nelle reti di riferimento europee per garantire standard di cura omogenei e accesso alla ricerca clinica avanzata.
- Reti di Riferimento Europee (ERN):
- ERNICA: https://ern-ernica.eu/ (Anomalie digestive e gastrointestinali rare).
- ERN-LUNG: https://ern-lung.eu/ (Malattie respiratorie rare).
- PDTA Regionali (Esempi di riferimento):
Faq primarie per Atresia Esofagea
- Quali sono i principali fattori di rischio per la morbilità digestiva a lungo termine?
I fattori chiave includono la presenza di fistola tracheoesofagea distale, la condizione di “long-gap” (ampia distanza tra i monconi) e lo sviluppo di complicanze postoperatorie precoci.
- Come distinguere i sintomi respiratori associati all’asma da quelli legati alla tracheomalacia?
Mentre l’asma è un’infiammazione delle vie aeree inferiori, i sintomi respiratori nell’AE derivano spesso dalla stabilità meccanica ridotta della trachea (TM). Test funzionali come la spirometria con reversibilità sono necessari per confermare l’asma.
- Qual è la frequenza raccomandata per il monitoraggio endoscopico?
Le linee guida ESPGHAN-NASPGHAN suggeriscono monitoraggi regolari con pH-impedenzometria ed endoscopie seriali con biopsie, specialmente per identificare precocemente l’esofago di Barrett, data la scarsa correlazione tra sintomi e danno mucoso.
- Cosa fare in caso di crisi di “blue spells” nel lattante?
Questi episodi di cianosi improvvisa sono spesso legati a tracheomalacia severa durante l’alimentazione o il pianto. Richiedono valutazione urgente per eventuale supporto ventilatorio (CPAP) o interventi chirurgici come l’aortopessi.
No metadata found.